Alpha1-antritrypsin (AAT) deficiency is a genetic disease
AAT is a protein encoded by a gene known as SERPINA11. There are many genetic variants, or alleles, of SERPINA11 but the ones most commonly associated with severe deficiency include the PiS, PiZ and Pi(null) alleles.1,2
The most common SERPINA1 (Pi) alleles*,†1,2
| SERPINA1 alleles | Protein phenotype |
|---|---|
| PiM | Normal |
| PiS | Protein is degraded in cells |
| PiZ | Protein accumulates in cells |
| Pi(null) | No protein is made |
AAT deficiency is an autosomal recessive disease caused by the inheritance of two deficiency alleles of SERPINA1, which results in a deficiency of AAT protein in the serum and lungs.1,2
AAT deficiency is one of the world's most prevalent and serious inherited disorders3,4
AAT deficiency — not as rare as you thought
Inheritance patterns of AAT deficiency
Example 1:
If one parent has two PiM alleles (PiMM genotype) and another parent has two PiZ alleles (PiZZ genotype), 100% of their children will be heterozygous carriers of the PiZ allele.
| hide | hide | GENOTYPE PARENT 1 | |
|---|---|---|---|
| hide | hide | PiM | PiM |
| GENOTYPE PARENT 2 | PiZ | PiMZ | PiMZ |
| PiZ | PiMZ | PiMZ | |
Example 2:
If both parents are heterozygous carriers of PiZ (genotype MZ), there is a 25% chance of a child having AAT deficiency (genotype PiZZ), a 50% chance of a child being a heterozygous carrier (genotype PiMZ) and a 25% chance of having the “normal” genotype (genotype PiMM).
| hide | hide | GENOTYPE PARENT 1 | |
|---|---|---|---|
| hide | hide | PiM | PiZ |
| GENOTYPE PARENT 2 | PiM | PiMM | PiMZ |
| PiZ | PiMZ | PiZZ | |
Serum testing alone is not a diagnostic tool for AAT deficiency
Although the average concentration of serum AAT is associated with genotype (see Relationship between genotypes and average serum AAT concentrations), AAT levels fluctuate because it is an acute phase protein.5
Therefore, there is overlap in the average concentrations between genotypes, particularly if the deficiency is intermediate so that serum testing alone is insufficiently specific to diagnose AAT deficiency.5 In addition, serum testing may overestimate AAT concentrations by as much as 35-40%.2
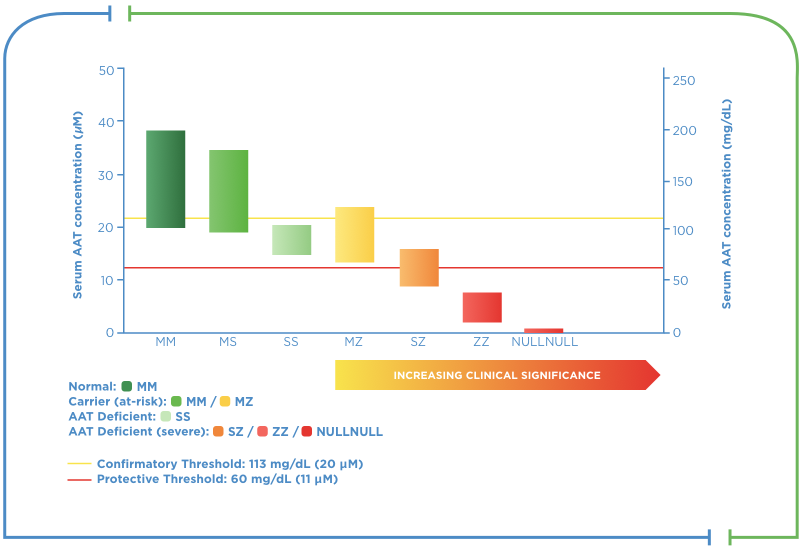
Relationship between genotypes and average serum AAT concentrations‡
Range of serum AAT levels by phenotype
Laboratory testing (such as testing via genotyping and phenotyping) is the only way to accurately diagnose AAT deficiency.1
References
- Köhnlein T, Welte T. Alpha-1 antitrypsin deficiency: pathogenesis, clinical presentation, diagnosis, and treatment. Am J Med. 2008;121(1):3-9.
- ATS, ERS. American Thoracic Society/European Respiratory Society statement: standards for the diagnosis and management of individuals with alpha-1 antitrypsin deficiency. Am J Respir Crit Care Med. 2003;168(7):818-900.
- de Serres FJ. Worldwide racial and ethnic distribution of alpha1-antitrypsin deficiency: summary of an analysis of published genetic epidemiologic surveys. Chest. 2002;122(5):1818-29.
- Campos MA, Wanner A, Zhang G, et al. Trends in the diagnosis of symptomatic patients with alpha1-antitrypsin deficiency between 1968 and 2003. Chest. 2005;128(3):1179-86.
- Miravitlles M, Dirksen A, Ferrarotti I, et al. European Respiratory Society statement: diagnosis and treatment of pulmonary disease in α1-antitrypsin deficiency. European Respiratory Journal. 2017;50(5).
- Vidal R, Blanco I, Casas F, et al. Guidelines for the diagnosis and management of alpha-1 antitrypsin deficiency. Arch Bronconeumol. 2006;42(12):645-59.
- Topic A, Alempijevic T, Milutinovic AS, et al. Alpha-1-antitrypsin phenotypes in adult liver disease patients. Ups J Med Sci. 2009;114(4):228-34.
- Teckman JH. Liver disease in alpha-1 antitrypsin deficiency: current understanding and future therapy. COPD. 2013;10 Suppl 1:35-43.



genotypes sups
*There are over 100 identified alleles of SERPINA1, including many that produce no AAT (“null” alleles).1,2
†The PiZ allele results in AAT intracellular polymerisation, which may lead to liver cell injury and death. The PiS allele results in rapid intracellular degradation of AAT. The PiS allele is associated with a milder AAT deficiency and increased risk of liver disease when it is co-inherited with PiZ (e.g. PiSZ).7,8
‡The maintenance of blood serum levels of alpha1 antrypsin (AAT) proteinase inhibitor (Pi) (antigenically measured) above 11 μM (or 80 mg/dL by radial immunodiffusion), considered a protective threshold, has been historically postulated to provide therapeutically relevant anti-neutrophil elastase protection, although this has not been proven.2 A confirmatory threshold of 20 μM (113mg/dl) of AAT will detect PiMZ, PiSZ, PiMS and PiSS with high sensitivity and specificity.
AAT: alpha1 antitrypsin.